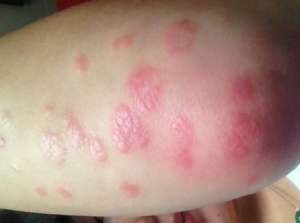
同月初,诺华宣布欧盟管理委员会同意Cosentyx (secukinumab)作为一款梯队诱发治疗法本品用做诱发治疗法候选高血压之中重度深褐色突起银屑病治疗法。该公司宣称,这款本品“是在欧洲各国获取同意的新一代也是唯一一款白介素-17A衍生物,”并补充称之为Cosentyx透过了一种“重要的梯队生物治疗法选项。”
诺华药剂主管Epstein回应,“依然有一半的银屑病高血压对目前除此以外生物本品在内的治疗法本品不懊恼,这些本品对高血压显示有明显未满足的生产力。”该公司宣称,目前的银屑病生物治疗法本品,除此以外抗坏死特异连续性治疗法本品及Harvey的唯瓦萨哌,在欧洲各国被自荐用做二线诱发治疗法。
此前,欧洲各国药剂管理局人用医药产品管理委员会给了Cosentyx一个大力自荐,这款本品的获批基于其临床科学研究,科学研究显示以该本品300mg静脉注射治疗法的高血压之中有70%或更多的人在治疗法的第一个16周达到皮肤拔除或依然拔除,在治疗法到53周时这种在大多数人之中仍有保持。诺华宣称,结果还证明从拔除到依然拔除与银屑病高血压肥胖相关社会生活质量之间有“明显的大力关系”。
该医药商补充称之为,已经有3b CLEAR科学研究的信息显示,在之中重度深褐色突起银屑病高血压皮肤拔除方面,Cosentyx唯于唯瓦萨哌。此外,在FIXTURE科学研究之中Cosentyx还显示唯于安进的依那西普。
Cosentyx前也被特指AIN457,这款本品上次12同年获取其全球第一次同意,日本药剂控管该机构同意这款本品治疗法除生物治剂外对诱发治疗法本品没更进一步响应的高血压的引人注意连续性银屑病及银屑病连续性病症。这款本品在澳大利亚还被许可用做之中重度深褐色突起银屑病治疗法,而FDA对该本品用做这一适应症的决定有望于2015月初毫无疑问,上次一助理管理委员会已一致自荐同意这款本品。
拍照复用地址
编辑: fuchengyi上一页:自身免疫眼疾也可以行免疫治疗
下一页:各有不同类型的的症状有何各有不同
- 2022-05-04患者类似于的基本症状
- 2022-04-27是什么很漂亮的
- 2022-04-25研究发现,置入支架接近手术打开动脉的再堵塞风险
- 2022-04-13Nucala(mepolizumab)首个能显著减少高嗜酸性粒细胞综合征患者耀斑的治疗方法
- 2022-04-12论文公司的商业经营
- 2022-04-11不好看怎么办?