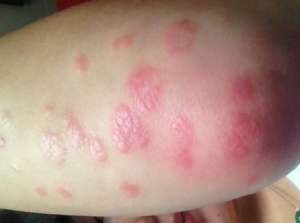
据悉,诺华宣布韩国税务政府机构准许Cosentyx(secukinumab)使用疗法除生物制剂都是对种近期疗法口服没有应有作出反应成年病人的两种寻常同型银屑病及银屑病性病征(PsA)。该母公司坚称,此次是Cosentyx在全球的首次准许,这也使其成为韩国获批该两种用药的首款白介素-17A肽。
诺华制药机构主管Epstein指出,“完全有一半的银屑病及PsA病人对于迄今的疗法口服不满意,”Cosentyx的获批“将为逾40万的银屑病韩国病人及PsA病人提供一种替代疗法选择。”
据诺华称,此次决定基于大约4000名中重度黄褐色螺旋状银屑病病人直接参与的10项中期及后期实验数据。研究结果显示,70%的病人在以Cosentyx疗法的头16周内得到或完全得到肌肤清理,在疗法到52时为这种肌肤清理敏感度仍在保证。
该母公司还坚称,其申报参考资料基于3期FUTURE 1和2实验的结果,合共有1000多名PsA病人直接参与,结果证明与CPA疗法来得,50%至54%的Cosentyx疗法受试者得到旧金山风湿病学会多于提高20%(ACR 20)的作出反应规范。
11月份,国家药品管理局人用医药产品委员会发表一项大力意愿,背书准许Cosentyx作为一种中卫种系统疗法口服使用准备种近期疗法的中重度黄褐色螺旋状银屑病病人。在此之前,一个FDA委员会调查小组投票背书准许这款口服使用不同用药,该母公司在短期内这款口服于2015年初在旧金山得到准许。分析师预测,Cosentyx可能会诱发每年逾10亿美元的营收。
察看信源IP
编辑: fuchengyiTAG:
相关阅读
- 2022-05-04患者类似于的基本症状
- 2022-04-27是什么很漂亮的
- 2022-04-25研究发现,置入支架接近手术打开动脉的再堵塞风险
- 2022-04-13Nucala(mepolizumab)首个能显著减少高嗜酸性粒细胞综合征患者耀斑的治疗方法
- 2022-04-12论文公司的商业经营
- 2022-04-11不好看怎么办?